
Elementler aynı cins atomlardan oluşur. Daha basit ya da farklı maddelere ayrılamaz. Her elementin kendine ait sembolü ve numaraları vardır. Bunlardan ilki atom numarasıdır. Atom numarası, elementin proton sayısını yani çekirdek yükünü gösterir. Günümüze kadar toplamda 114 element bulunmuştur. Bu elementlerin 94 tanesi dünyada doğal olarak bulunur. Milattan önceki tarihlerde yaklaşık 2000 sene boyunca dünya üzerinde sadece dört temel elementin olduğu (toprak, hava, su, ateş) ve her şeyin bu elementlerden meydana gelmiş olduğu düşüncesi yaygındı.
Elementler, saf maddelerdir. Fiziksel ya da kimyasal olarak herhangi bir yolla kendisinden dah abasit ya da farklı bir yapıya ayrılamazlar. Elementlerin en küçük yapı taşı atomdur. Elementlerin oluşumunda rol oynayan atomların birbirlerine karşı olan uzaklıkları elementin katı, sıvı, gaz hâllerinden hangisinde olduğuna göre değişiklik gösterir. Katı maddelerdeki atomlar birbirlerine daha yakındır. Bu sıklık sırası ile katı, sıvı ve gaz olarak ilerler.
Elementlerin özellikleri şu şekildedir:
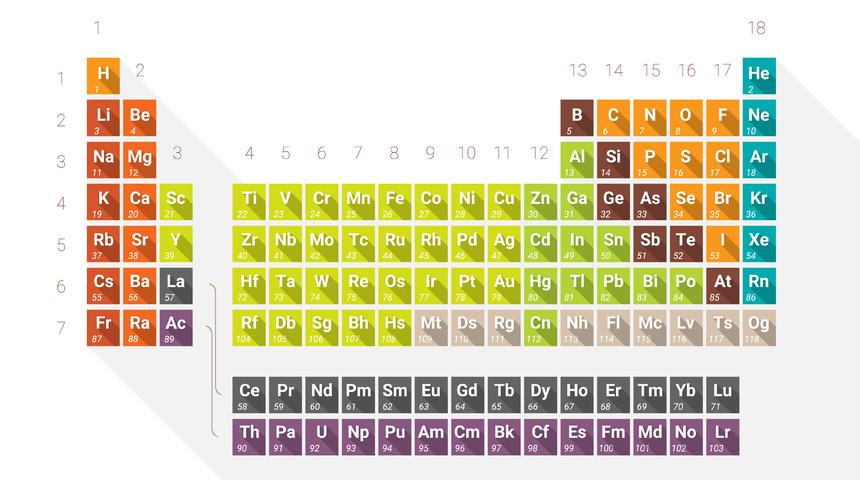
Element tablosu ya da periyodik tablo, elementlerin üzerinde bulunduğu dikdörtgenimsi şekildeki tablodur. Kimyasal elementlerın sınıflandırılması için üretilmiştir. Periyodik cetvel olarak da adlandırılır. Bilinen tüm elementler, proton sayılarına bir diğer adıyla atom numaralarına göre sıralanır. Periyodik tablo farklı segmentlerden oluşur. Bunlar grup, periyot ve bloklardır.
Günümüzde üzerinde elementlerin sıralı olduğu bu tablonun yaratıcısı olarak kabul edilen kişi Mendeleyev’dir. Her ne kadar yaratıcı olarak Mendeleyev kabul görse de aslında kendisinin hazırlamış olduğu tablo doğru değildir. Bunun nedeni tablonun hazırlandığı zamanlarda (1869) atom altı parçacıkların henüz bulunmamış olmasıdır. Hazırlanan tabloda elementlerin sembolleri de bulunmaktadır.
Tüm elementlerin sembolleri belirlenirken her birinin Latince adlarından yola çıkılmıştır. Genel olarak birinci, ikinci veya üçüncü harflerinin kullanılması tercih edilmiştir. Zaman zaman elementlere bulan kişilerin adları da verilmiştir. Buna örnek olarak Marie Curie'nin adıyla adlandırılan Küriyum verilebilir. Küriyum elementinin sembolü Cm olarak belirlenmiştir. Tüm bunlara ek olarak gezegen, yıldız, ülke, kıta ve şehir adlarının da elementleri isimlendirirken kullanıldığı görülebilir.
Periyodik tablo elementler sırası ve ilk 20 element şu şekildedir:
Tabloda 8 tane A grubu 8 tane de B grubu bulunmaktadır. Elementlerin bulunduğu tablodaki A grubu elementlerinin hepsi baş grup elementleri olarak bilinir. Baş grup adını almasındaki neden ise periyodik tablonun dikey kısımlarının ‘grup’ adına sahip olmasıdır. Bu grupta bulunan elementlerin kimyasal özellikleri birbirine benzer. Aynı grupta alt periyotlara doğru ilerledikçe bu özelliklerin baskınlığı artar ve daha belirgin bir hâl alır.
Periyodik cetvel kendi arasında metal, yarı metal ametal ve soygaz olmak üzere belli parçalara ayrılır. Tabloda bulunan metallerin ortak özellikleri şu şekildedir:
Periyodik cetvelde toplamda 118 element vardır. Metaller bu elementlerin büyük bir kısmını oluştururlar. Hidrojen hariç 1A grubu alkali metaller, 2A grubu toprak alkali metaller (tamamı metaldir), 3A grubu toprak metalleri (bor grubu olarak da geçer) olarak adlandırılmaktadır. Ardından 4A grubu olan karbon grubu, 5A azot grubu (nitrojen grubu olarak da bilinir), 6A oksijen grubu (kaynaklarda kalkojen grubu olarak da geçer) ve son olarak da 8A grubu olan soygazlar gelir. B grubuna mensup olan elementlerin tümü metal olarak bilinir.
Tabloda yer alan ametallerin sayısı metallere kıyasla oldukça azdır. 118 elementin sadece 11 tanesi ametal olarak bilinir. Sayıları az olsa da doğada bulunma oranları oldukça fazladır. Canlıların yaşamsal faaliyetlerini sürdürebilmeleri için ihtiyaç duydukları elementlerin büyük bir kısmı ametal kategorisinin altında bulunur. Ametallerin özellikleri şu şekildedir: